[がん治療の現状と課題]日本最大のがん治療センターから #01
連載:[がん治療の現状と課題]日本最大のがん治療センターから
2024.12.09
放射線治療の先駆者である秋元先生にお話を伺う本連載、1記事目となる本記事では、がん治療の基礎知識や病院側の医療体制から、現場医師が感じる現時点での技術的限界にもお話を広げます。
――取材協力:秋元哲夫氏――

昭和61年3月 群馬大学医学部卒業
平成元年6月 国立がんセンター中央病院 レジデント
6年5月 群馬大学医学部放射線科 助手
9年2月 米国MD Anderson Cancer Center, Dept. of Experimental Radiation Oncology 留学(〜平成10年3月)
13年4月 群馬大学医学部放射線科 講師
18年7月 東京女子医科大学 准教授
22年7月 臨床教授
23年7月 国立研究開発法人 国立がん研究センター 東病院
臨床開発センター粒子線医学開発分野分野長(放射線治療科長併任)
26年5月 国立研究開発法人 国立がん研究センター東病院 副院長
27年6月 放射線品質管理室 室長併任
順天堂大学大学院 客員教授
東京女子医科大学 客員教授
東京慈恵医大大学院 客員教授
明治薬科大学 客員教授
平成30年9月 レディースセンター センター長併任
平成31年2月 人材育成センター センター長併任
日本放射線腫瘍学会 認定医
日本医学放射線学会 専門医
――放射線治療はがん治療においてどのような位置付けなのでしょうか?
がん治療には、手術、お薬、放射線治療という三大治療がありますが、放射線治療はその中の1つです。近年はここに免疫療法が入ってきています。
以前はがんの腫瘍の位置を正確に把握することは難しく、根治を目指す上では手術とお薬が主流でした。放射線療法はあくまでそれらが使えない患者さんに対して、次の選択肢として位置付けられていたんです。その認識が2000年代当初くらいまで続いていました。
しかし、40年ほど前にCTが普及し始め、さらにコンピューター技術が発展したことで、がんの位置を正確に特定して照射できるようになってきました。これが放射線治療によって「治す」ことを可能にしたんです。そうして「3大治療」の時代になってきたのが2000年代初めの流れです。
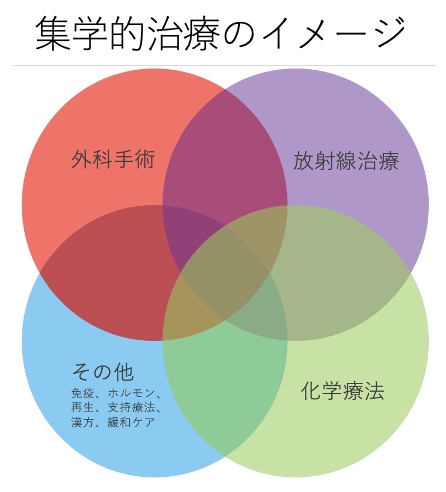
それまでは放射線治療と抗がん剤の治療が独立に行われてきましたが、薬物治療の進歩も相まって、徐々に放射線治療と薬物療法を並行して取り組むことで治療効果が高まることが分かってきました。そのように、集学的治療といって、手術と薬物治療と放射線治療を組み合わせるという概念が一般的になりました。
――放射線治療の発達は、正確な照射技術の発達に集約されるということでしょうか。
そうですね。これは、放射線が正常な組織に当たってしまうと副作用が現れるからです。例えば肺がんを治療すると照射した皮膚が赤くなったり、がんの患部の近くに食道や粘膜があると粘膜炎が現れたり、頭部に当たると脱毛状態になったりします。
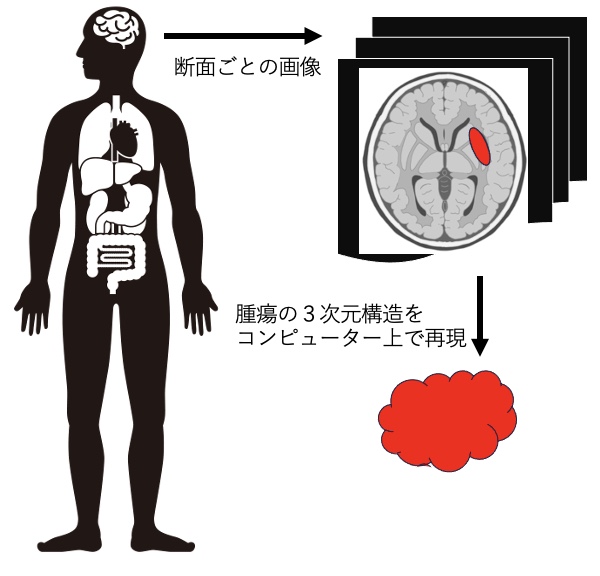
これを抑えるために、腫瘍の位置を3次元で正確に捉えて多方向から照射するような技術が発達してきました。昔はX線で患者さんの患部を1方向から透視して位置を捉えていたんですが、最近は患部を輪切りにしたようにたくさんの断面で画像を得られるようになっています。これをコンピューターで処理して3次元に構成し直すことで、立体的な形に再構成できるようになったんです。
完全に正常組織への影響をなくすことはできないので副作用はありますが、年々減ってきています。
さらにコンピューター技術の進歩によって正確な照射ができることで、臨床成績は向上し続けています。現在は手術に比べてあまり遜色ない治療成績が出せるがん種も増えてきています。
――どの方向からどれくらい照射するかを最適化するのは完全にコンピューターの処理で行うのですか?
医療者とコンピューターの分業の仕方は、時代と共に変わってきたところです。がんの位置を3次元で把握できるようになった初期は、照射する方向を人間が決めていました。これをフォワードプランニングと言います。しかしそれだと、当て方は決める人の経験や考えに左右されてしまいますよね。そこで近年は、患部とその周辺に対して、この場所にはこれくらいの線量までを入れたいという数値を入力することで、どの方向からどのように照射するかをコンピューターが計算して最適化してくれるようになりました。これをインバースプランニングといいます。つまり、昔は自分達が解を出していましたが、最近はコンピューターに解を出させるための条件を私たちが入れるようになったということです。
――どの病院のどの医師が担当しても、コンピューターによって自動的に同じ照射方法が提案されるのでしょうか?完全に最適化されていると言ってよいのか、それともアルゴリズムの部分などでまだ改善が見込めるものなのかはどうお考えですか?
改善できる部分や人の手を加えるべき部分はまだ多くあります。コンピューターから出てきた解に対しても、そのまま鵜呑みにするのではなく、さらに改善できると判断されれば入力を変えてやり直すことがあります。
効果と副作用は一般にトレードオフで、片方を高めるにはもう片方を譲歩するしかないという関係にあります。ある患者さんの特定の部位について、効果と副作用のどちらをどれくらい優先するかという判断は難しく、コンピューターで計算できるような、一概に言える正解があるわけではないんです。それは医療者の経験と、患者さんとのコミュニケーションによってバランスを見極めるしかありません。患者さんを目の前にして、これを治すためにこの部分の副作用は目を瞑ろうと考える時もあれば、この部分の副作用は許容できないので効果が下がっても線量を下げようといったことを考える時もあります。
――コンピューターにも限界があるということなのですね。
そうです。今はまだできないことは色々あります。例えばAIの応用もそうです。人間の臓器の位置や接続といった解剖学的な知識はAIに学ばせることができても、がんの位置をトレースさせるところは事前に学ばせることができないですよね。がんの形は必ず患者さんによって異なりますから。よって、どこまでをがんとみなすか、どこからを正常な腫瘍とみなすかはAIにはできていません。
画像というのは、一定の条件を満たした部分かどうかで濃淡をつけているだけです。しかしがん細胞というのは、実は画像化できるものではありません。周辺にがん細胞が広がっているという時に、どこまでがんが浸潤しているか(広がっているか)というのは、経験の中でわかってくるものなんです。こういうがんに対して、こういうふうに治療したらこういうところに再発しました、というような経験が積み重なることで、どうもこの部分に再発する人が多いが、その外側まで照射範囲を広げるとさのサイズが減ったんだということが見えてくるんです。AIで自動化できる作業がかなり増えてきた中でも、今の段階ではまだまだ完全な自動化には遠いという一例です。
――経験が重要なのですね。若い先生が主導して治療することはないのでしょうか。
はい。照射のしかたについては経験のあるスタッフによるダブルチェックが入ります。より広い意味では、一つのがんを外科や内科や放射線治療などの他分野の先生が関わって治していく、集学的治療が今の時代のやり方になっているので、単独の先生が決めるというイメージではありません。当センターもカンファレンスといって、外科、内科の先生と私たち放射線科の医師やCTのような診断を担う先生が集まって、この患者さんはこの範囲のこういう治療が適切だろうといった検討を行います。若い先生たちもここに出席して、ディスカッションを見ながら学ぶ機会になっています。

――最適な治療法を話し合う際には意見が分かれることもあると思いますが、診療科同士の連携に難しさはありませんか?
その判断は、基本的に患者さんに委ねられます。カンファレンスで多方面の専門家が集まると選択肢は必ず複数上がってきます。このとき、議論の目的は治療法を一つに絞ることではなくて、複数の適した選択肢を挙げて患者さんに説明することです。
昔は医師が治療法を決めてしまう時代もありましたが、今の主流はインフォームドコンセントといって、医師が患者さんに病気のことや選択肢を伝えるやり方です。例えば、AとBの2つの治療方法を考えた時に、治療成績はAが一番いいが、Bは体への負担が少なくなる、ということもあります。がんの知識がない患者さんにとっては非常に難しい選択に感じられるかもしれませんが、今は昔と違って患者さんがインターネットを通じて色々な情報を得られるようになってきました。したがって、選択肢を提示してからその場で決めさせるのではなく、しっかり調べて納得できる選択をしてもらうようにしています。
この決定プロセスは欧米で始まったもので、シェアードディシジョンメイキング(Shared Decision Making)といいます。いろいろな情報を、複数の診療科の医療者と患者さんとご家族でシェアした上で、最終的に決定するということです。
オーストラリアや欧米では、複数の選択肢が上がった時には、必ずそれぞれの専門家から話を聞いてから方針を決めないと保険でカバーしないというルールが提案されています。例えば外科の先生が外科手術を勧めて治療してから、後になって実は放射線治療や薬物療法もあったことを知るということを防ぐためです。この説明のためには、医療者側も口頭ではなくて書面で説明書を作るというのが主流になってきています。さらに、医師と診察室にいる時には緊張してしまって質問が浮かばなかったり訊けなかったりすることも多いので、説明を受けた後に看護師さんに相談できる看護外来というところもあります。そこで出た質問や疑問は医師にフィードバックされることで、説明も改善されていくという体制になっているんです。
<国立がん研究センター 東病院>
ホームページ:https://www.ncc.go.jp/jp/ncce/index.html
所在地:〒277-8577 千葉県柏市柏の葉6-5-1
TEL:04-7133-1111(代表)



![[がん治療の現状と課題]患者の懸念、医療制度の課題 #02](https://doctor-journal.com/wp-content/uploads/2024/01/f921745e9e011d0f14238fc3803310b9-640x320.png)
![[がん治療の現状と課題]放射線治療の課題、秋元先生の取り組み #03](https://doctor-journal.com/wp-content/uploads/2024/02/06e0d7d2282c5b5f17ff718a92ca8b70-640x320.png)
![[がん治療の現状と課題]日本最大のがん治療センターから #01](https://doctor-journal.com/wp-content/uploads/2023/12/44cbbfe318163c500ed08498f8d602c8-640x320.png)




































![[がん治療の現状と課題]放射線治療の課題、秋元先生の取り組み #03](https://doctor-journal.com/wp-content/uploads/2024/02/06e0d7d2282c5b5f17ff718a92ca8b70-80x80.png)
![[がん治療の現状と課題]患者の懸念、医療制度の課題 #02](https://doctor-journal.com/wp-content/uploads/2024/01/f921745e9e011d0f14238fc3803310b9-80x80.png)